第4回プロテオミクスシンポジウム
「個別疾患ごとに最適化した疾患プロテオーム研究
~医学部と理学部の共同研究ネットワーク~」
北里大学理学部物理学科生体分子動力学講座 講師 大石 正道
(1) はじめに
「疾患プロテオミクス」の最終的な目的は医学への貢献である。具体的には、二次元電気泳動法やHPLC法、あるいは質量分析法などのプロテオミクス技術を用いて、疾患関連タンパク質(あるいはそのペプチド断片)の分離・精製、次に正常臓器と疾患臓器のプロテオームの比較解析、最後に発現量に変動の見られた疾患関連タンパク質の同定を行うことが、疾患プロテオミクスの常道とされてきた。医学分野からの疾患プロテオミクスへの期待は、疾患マーカータンパク質の探索に始まり、プロテオーム解析による疾患発症のメカニズム解明、特異抗体を用いた疾患診断用ツールの開発、さらには創薬ターゲットの探索など多岐にわたっている。
我々が1994年から2006年までに行ってきたさまざまな共同研究から得られた教訓は、個別疾患ごとに目的達成のために最適化した手段を用いた研究を行う必要があるということである。すなわち、早期腫瘍マーカーに乏しい膀胱癌の場合、血清や尿検体におけるマーカーの探索と臨床検査用に最適化したアッセイ系の確立が重要なテーマになる。一方、糖尿病では、活性酸素によるDNAやタンパク質の酸化傷害が症状の程度を示すマーカーになるため、タンパク量の増減だけを調べていても、酸化傷害という重要な情報は逃してしまう。従って、タンパク質の酸化傷害の程度も含めて検討しなくてはならない。
(2) 共同研究の草の根ネットワークと北里疾患プロテオーム研究会
我々の研究グループは、北里大学医学部、医療衛生学部、薬学部、水産学部、北里生命科学研究所などとさまざまな形態で共同研究を行ってきた。さらには、千葉大学医学部分子病態解析学教室との共同研究は密接で、研究セミナーやシンポジウム、大学院生の研究交流などを行っている。これらの共同研究ネットワークは自然にできあがったものであり、研究計画に無理やり個々の研究グループをはめこんだものではない。従って、我々はこれらの気の合った仲間同士の連携を「草の根研究ネットワーク」と呼んでいる。
M.D.とPh.D.はそれぞれ互いに異なる知識と経験を持ち、互いに補い合う関係にあると考えている。現在、我々の研究室にはPh.D.とM.D.が一緒に机を並べて研究できる体制が実現でき、率直な意見交換ができる場が形成されている。
疾患プロテオーム解析で何ができるか、またどのような方法で行うのかについて、北里大学内で啓蒙活動を行うために、2003年から毎年、「北里疾患プロテオーム研究会」というシンポジウムを行ってきた。昨年からは北里大学内だけでなく一般に公開して行っている。2006年8月4日(金)には、北里大学相模原キャンパスにおいて第4回北里疾患プロテオーム研究会を行い、口頭発表6演題(招待講演と教育講演を含む)、ポスター発表32演題、およびプロテオミクス関連企業によるブース展示22社の3本柱で行った。この研究会には200名を超える参加者があった。各講演に関して積極的な質疑応答があり、ポスタープレゼンテーションの1時間半の間には、研究者どうしの積極的な意見交換や、プロテオミクス関連企業による新規プロテオミクス関連技術の紹介などがあり、たいへん盛況な一日であった。
(3) アガロース二次元電気泳動法(アガロース2-DE)による疾患プロテオーム解析例:遺伝性小人症ラットrdwのプロテオーム解析
1994年、前田忠計教授の提案によって、大石の持つアガロース二次元電気泳動法と三菱化学(株)生命科学研究所の大森彬研究員の微量タンパク質アミノ酸配列解析法との組み合わせとが、疾患関連タンパク質の分離・同定に役立つことがわかり、現在我々が積極的に進めている「疾患プロテオーム解析」の原型ができあがった。1994年はプロテオームという用語ができた年でもあり、我々は2年後にその言葉を知るまで、プロテオームという言葉を知らずに同じ解析方法を行っていたことになる。
1996年からは医学部実験動物学の古舘専一助教授との共同研究「遺伝性小人症rdwラットの疾患プロテオーム解析」が始まった。rdwラットは典型的な成長障害を引き起こすが、成長ホルモン遺伝子およびその転写調節因子であるPit-1の遺伝子には変異は見つからず、分子生物学的手法では、原因臓器および原因遺伝子の探索は不可能な状況だった。古舘助教授からの依頼を受け、大石がrdwラットの30種もの臓器についてアガロース2-DE法で調べたところ、甲状腺でのみ顕著な異常が認められた。すなわち、甲状腺では数十種類ものタンパク質成分に異常な蓄積が認められ、それらを同定した結果、いずれも小胞体の分子シャペロンタンパク質であることが明らかになった。甲状腺以外の臓器では小胞体分子シャペロンの異常蓄積が認められなかったことから、甲状腺特異的分泌タンパク質として知られるチログロブリン(甲状腺ホルモンの前駆体)に異常があることが示唆された。独協医大の菱沼昭助教授によってチログロブリン(Tg)のアミノ酸配列に1ヶ所塩基異常が見つかり、それがこの疾患の原因であることが明らかになった。すなわち、Tgのアミノ酸配列異常が、正常な立体構造形成を狂わせて、分子シャペロンがTgに結合したまま異常蓄積され、Tgの加水分解によって生じるはずの甲状腺ホルモンがほとんどできず、血中の甲状腺ホルモン量低下によって下垂体の成長ホルモン量の低下を招いたことが明らかになった。(この研究内容はEndocrinologyに2報(1998年と2000年)発表した)
(4) 糖尿病における酸化傷害プロテオーム解析
我々は、2000年から2004年まで、前田忠計教授が研究代表者となって文部科学省科学研究費特定研究「ゲノム医科学」の計画研究班に所属し、「プロテオームによる糖尿病の病態解析法の確立」をテーマに、糖尿病モデル動物および糖尿病患者血清を用いて、糖尿病関連マーカー探索を目的にアガロース2-DEと質量分析計を組み合わせたプロテオーム解析を行った。小寺義男講師がイオントラップ型質量分析計LC-MS/MSを立ち上げ、現在では一日に約80個のスポットを同定できる環境が整っている。研究を開始した当初は、アガロース2-DEを蛍光ディファレンシャル二次元電気泳動法(2D-DIGE)と組み合わせて糖尿病モデルラットOLETFを用いて発現プロテオミクスを行っていたが、優れた疾患マーカーが見つからなかった。糖尿病では活性酸素によるDNAやタンパク質の酸化傷害が糖尿病の病態に深く影響することを知り、カルボニル化タンパク質を特異的に検出する酸化傷害タンパク質検出法を開発した(Free Radic. Biol. Med, 2003)。この方法を用いて糖尿病ラット骨格筋と心筋を調べたところ、コントロールに比べて、ミオシン重鎖、アクチン、クレアチンキナーゼなどのタンパク質が酸化傷害を受けていることを発見した。このことから、糖尿病の病態解析には、発現プロテオミクスだけでは不十分で、タンパク質の酸化傷害に伴う機能喪失を調べる機能プロテオミクスも調べることが必要であることがわかった。
(5) 各種癌(前立腺癌、消化器癌など)の高分子プロテオーム解析による新規腫瘍マーカー候補の探索
2002年から2006年にかけて、北里大学医学部泌尿器科の馬場志郎教授らの研究室と共同で、前立腺癌、膀胱癌、腎臓癌の早期診断用マーカー候補タンパク質を探索するため、培養細胞、患者からの手術検体、患者血清、および患者尿を用いて、プロテオーム解析を行った。ヒト前立腺癌細胞LN-CaPのプロテオーム解析では、アガロース2-DEが分子量10万以上の高分子量タンパク質が解析できる利点を生かして、新規腫瘍マーカー候補を約30個発見した。その中には転写・翻訳関連因子が多く含まれていた(Kuruma et al., Proteomics 2005)。その後、膀胱癌の早期腫瘍マーカー探索のために、尿タンパク質の濃縮・脱塩法を開発し、タンパク尿マイナスの健常人の尿のアガロース2-DEパターンを作成し、そこから200個ほどのタンパク質を同定した。現在は、膀胱癌患者の尿タンパク質のプロテオーム解析を行っている。一方、腎細胞癌についても患者手術検体を用いてプロテオーム解析を進めており、これまでに癌に特異的な約200個のタンパク質の同定に成功した。
一方、千葉大学医学部分子病態解析学研究室の野村文夫教授、朝長毅助教授らとの共同研究では、アガロース2-DE法とLC-MS/MSとの組み合わせにより、消化器癌(大腸癌: Tomonaga et al., Clin. Cancer Res.2005; 食道癌: Nishimori et al., Proteomics 2006)で多数の腫瘍マーカー候補タンパク質を発見した。
(6) 疾患プロテオミクスの展望
疾患プロテオミクスでは、まず医学関係者の明確な研究目的が必要で、その目的を達成するために、プロテオミクス研究者と一緒に研究当初から綿密な計画を練り上げることが重要である。また、疾患プロテオミクスでは疾患関連タンパク質を同定した後、その結果が病態とどのような関連があるのかを考察するのが難しい。従って、疾患プロテオミクスにおいては、発現プロテオミクスだけでなく、タンパク質の機能変化に着目した機能プロテオミクスも必要であり、そして何よりも「医学への貢献にもっとも近道と考えられる研究手段をとる」ことが大切であると考えている。
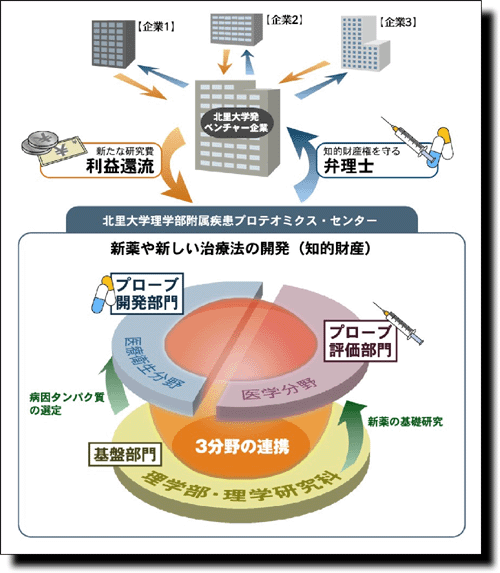
我々は医学により近道と考えられる「疾患診断に直結する抗体プロテオミクス」の重要性を認識して、2000年から疾患を診断するためのプローブづくり(主に特異抗体と分子プローブを使用)を開始した。2005年4月からは「北里大学理学部附属疾患プロテオミクスセンター(センター長:前田忠計教授)」を設立し、その中の3部門(疾患診断プローブ開発部門、プロテオミクス基盤部門および疾患診断プローブ臨床評価部門)で、主に肺癌患者の血清診断に有用な抗体の作出、抗体のスクリーニング、診断用ツールの開発を行っている。